مراحل پژوهش در علوم زیستپزشکی؛ از کشت سلول تا کارآزماییهای بالینی
مقدمه
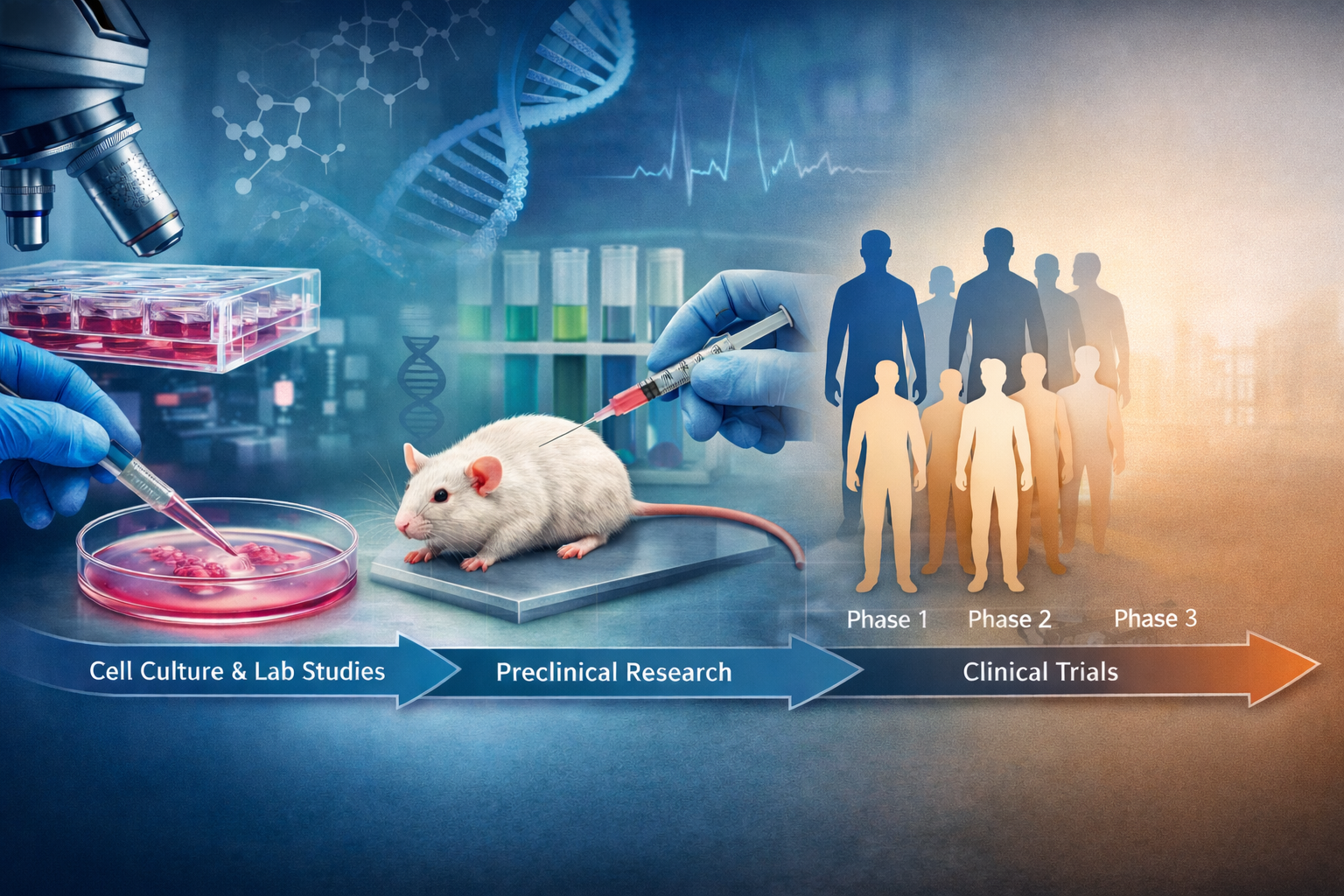
پژوهش در علوم زیستپزشکی و توسعه درمانهای جدید، یک مسیر علمی پیچیده و چندمرحلهای است. این مسیر از کشف هدفهای درمانی آغاز میشود، وارد فضای آزمایشگاه میگردد، سپس از طریق مطالعات پیشبالینی (شامل کشت سلولی و آزمایش روی حیوانات) عبور میکند و در نهایت وارد مراحل کارآزمایی بالینی روی انسان میشود. هدف از این فرآیند، یافتن درمانهای مؤثرتر، ایمنتر و علمیتر برای بیماریهاست. این مسیر بهصورت «از آزمایشگاه تا بالین» (Bench to Bedside) شناخته میشود و بخشی از فرایند استاندارد توسعه دارو و درمان در دنیاست.
۱. کشف و انتخاب هدف درمانی (Discovery & Target Identification)
اولین قدم در هر پژوهش زیستپزشکی یا توسعه دارو، شناسایی هدف مولکولی یا بیولوژیکی است. این هدف ممکن است یک آنزیم، گیرنده سلولی، مسیر سیگنالدهی، یا فرآیندی باشد که در بیماری خاص نقش دارد.
در این مرحله:
- دانشمندان با استفاده از دادههای ژنتیکی، بیوشیمیایی و زیستشناسی مولکولی، نقش اهداف بالقوه را در بیماری مطالعه میکنند.
- هدفهای درمانی جذاب انتخاب میشود و داروهای بالقوه – مانند مولکولهای کوچک، داروهای بیولوژیک، یا ایمونوتراپیها – طراحی میشوند.
این مرحله، مبنای علمی پژوهشهای بعدی است و لازم است بهخوبی حمایت شود تا نتایج مراحل بعدی قابل اعتماد باشند.
۲. مطالعات آزمایشگاهی In vitro — کشت سلولی و تستهای مولکولی
پس از انتخاب هدف، پژوهشها وارد فضای آزمایشگاه میشوند. در این مرحله، پژوهشگرها از سیستمهای آزمایشگاهی بدون حیوان استفاده میکنند تا اثرات اولیه دارو یا درمان را بررسی کنند.
کشت سلول (Cell Culture)
کشت سلول یکی از ابزارهای اساسی پژوهشهای زیستی است. در این روش:
- سلولهای انسانی یا حیوانی در ظروف آزمایشگاهی رشد داده میشوند.
- پژوهشگران میتوانند اثرات درمانهای جدید را بر رشد، تقسیم، مرگ یا سایر رفتارهای سلولی بررسی کنند.
کشت سلولی بهدلایل زیر ارزشمند است:
- کنترل محیطی دقیق: شرایط واکنش در آزمایشگاه کاملاً قابل تنظیم هستند.
- ارزیابی مستقیم اثرات دارو: پژوهشگران میتوانند تغییرات سلولی در پاسخ به دارو را بهطور مستقیم مشاهده کنند.
- پیشبینی نتایج اولیه: اگر یک ترکیب در سطح سلولی اثر ندهد، احتمالاً در مراحل بعدی نیز توجیه علمی کمی دارد.
در بعضی زمینهها از مدلهای پیچیدهتر «ارگانوئید» (organoids) یا سیستمهای چندسلولی استفاده میشود تا شباهت بیشتری به بافتهای واقعی بدن داشته باشد.
۳. مطالعات پیشبالینی (Preclinical Research)
اگر نتایج آزمایشگاهی نشان دهد که یک ترکیب یا درمان خاص مؤثر و بیخطر بهنظر میرسد، مرحله بعدی پیشبالینی است — که شامل آزمایش در مدلهای حیوانی و بررسیهای گستردهتر علمی میشود.
a. تعریف و اهمیت مطالعات پیشبالینی
مطالعات پیشبالینی به مجموعهای از آزمایشها گفته میشود که قبل از ورود به مطالعات انسانی انجام میشود. هدف اصلی این مرحله عبارت است از:
- تعیین ایمنی و سمیت بالقوه دارو.
- شناسایی دوزهای قابل قبول برای انسان.
- بررسی چگونگی رفتار دارو در بدن (جذب، توزیع، متابولیسم و دفع) — که بهاختصار PK/PD نامیده میشود.
طبق تعریف، مطالعات پیشبالینی شامل آزمایشهای درونتنی و برونتنی است:
- آزمایشهای In Vitro (برونتنی): شامل سلولها، بافتها یا سیستمهای مولکولی برای بررسی اثرات مستقیم دارو.
- **آزمایشهای In Vivo (درونتنی): استفاده از حیوانات آزمایشگاهی مانند موش، رت، خرگوش و غیره برای ارزیابی اثرات کامل دارو در موجود زنده.
b. مراحل و ارزیابیهای پیشبالینی
در مطالعه پیشبالینی، پژوهشهای زیر انجام میشود:
- بررسی اثربخشی اولیه: آیا ترکیب موردنظر اثر درمانی مطلوب را روی مدلهای بیماری دارد؟
- ارزیابی اعتبار مدل بیماری: بهکارگیری حیواناتی که شباهت بیشتری به بیماری انسانی دارند.
- مطالعات توکسیکولوژی (سمشناسی): تعیین حد دوزی که باعث ایجاد آثار مضر نمیشود.
- مطالعات PK/PD: بررسی چگونگی متابولیسم دارو و زمان باقیماندن آن در بدن.
- ارزیابی بیخطر بودن سیستم درمانی: برای خروج بدون خطر و قابل قبول برای تست در انسان.
در این مرحله، اگر نتایج مثبت باشند و خطرات مهمی شناسایی نشوند، تیم پژوهشی میتواند با ارائه دادههای علمی به سازمانهای نظارتی درخواست دهد تا اجازه دهد درمان وارد فاز کارآزمایی بالینی شود.
۴. آمادهسازی برای ورود به کارآزماییهای بالینی (IND / CTA)
قبل از شروع مطالعه روی انسان، باید به مراجع نظارتی در کشور مربوطه – مانند FDA در ایالات متحده – درخواست رسمی ارائه شود. این درخواست معمولاً بهصورت IND (Investigational New Drug) یا معادل آن در دیگر کشورها بهصورت CTA (Clinical Trial Application) ثبت میشود.
در این مرحله:
- دادههای مطالعات پیشبالینی جمعآوری میشود.
- طرح مطالعات بالینی (پروتکل) تهیه میشود که اطلاعاتی مانند معیارهای انتخاب شرکتکنندگان، روش دریافت دارو و نحوه پیگیری نتایج را مشخص میکند.
- تمام اطلاعات ایمنی و اثربخشی بالقوه دارو به سازمان نظارتی ارسال میشود.
سازمان نظارتی این دادهها را مرور میکند تا مطمئن شود پژوهش برای شرکتکنندگان انسانی بیخطر باقی بماند و معیارهای علمی مطلوب را دارا باشد.
۵. کارآزماییهای بالینی (Clinical Trials)
بعد از تأیید IND/CTA، پژوهش وارد مرحله بالینی میشود — یعنی آزمایش روی انسان. کارآزماییهای بالینی شامل مراحل یا «فازها» هستند که هر کدام اهداف مشخصی دارند و بهطور پیوسته اطلاعات بیشتری درباره ایمنی و اثربخشی درمان فراهم میکنند.
الف. فاز I — ارزیابی ایمنی و تعیین دوز
در این مرحله:
- درمان جدید برای اولین بار در انسان تست میشود.
- معمولاً تعداد کمی از شرکتکنندگان (۲۰ تا حدود ۱۰۰ نفر) حضور دارند.
- هدف اصلی، بررسی ایمنی، تعیین دوز قابل تحمل، و شناسایی عوارض جانبی اولیه است.
- اغلب شرکتکنندگان سالم هستند، مگر اینکه درمان مربوط به بیماریهای جدی باشد.
ب. فاز II — ارزیابی اثربخشی و بررسی ایمنی بیشتر
در فاز دوم:
- درمان روی گروه بزرگتری از افراد (معمولاً تا چندصد نفر) آزمایش میشود.
- هنوز ایمنی بررسی میشود، اما حالا تمرکز روی اثربخشی درمان در بیماران دارای بیماری هدف نیز قرار دارد.
- در این مرحله، دادههای بیشتری درباره اینکه درمان چگونه عمل میکند و به چه مقدار دوز نیاز است، جمع میشود.
ج. فاز III — مقایسه و تأیید نتایج
این مرحله، نقطه اوج کارآزماییهای بالینی است:
- درمان جدید با روش استاندارد درمان مقایسه میشود.
- شرکتکنندگان در این مرحله صدها تا هزاران نفر هستند.
- پژوهشگران عوارض جانبی کمتر شایع، اثربخشی واقعی درمان، و مزیت نسبت به درمان استاندارد را بررسی میکنند.
- یک فاز III موفق برای تأییدیه نهایی سازمانهای نظارتی جهت ورود به بازار ضروری است.
د. فاز IV — پس از ورود به بازار (Post-Marketing)
هنگامی که درمان تأیید شده و وارد بازار شد، پژوهش هنوز ادامه دارد:
- بهنام فاز IV یا Post-Marketing Surveillance انجام میشود.
- هدف آن شناسایی عوارض نادری است که ممکن است در فازهای قبلی دیده نشده باشند.
- اطلاعات مصرف واقعی در جمعیتهای گستردهتر بهدست میآید و میتواند منجر به توصیههای جدید درمانی شود.
۶. نقش طراحی و روششناسی در پژوهش
طراحی پژوهش، حتی در مراحل ابتدایی، یک عامل کلیدی برای اعتبار نتایج است. در کارآزماییهای بالینی:
- از طرحهای تصادفی کنترلشده (Randomized Controlled Trials) استفاده میشود تا اثرات واقعی درمان از تأثیرات تصادفی جدا شود.
- معیارهای دقیق برای انتخاب داوطلبان، کنترل گروه شاهد، و تحلیل دادهها بهکار میرود تا نتایج قابل اتکا باشند.
جمعبندی: از آزمایشگاه تا بالین
کل مسیر پژوهش زیستپزشکی و توسعه درمان عبارت است از:
- کشف هدف درمانی و طراحی مولکولها
- آزمایشهای In Vitro (کشت سلول) برای بررسی اثرات اولیه
- مطالعات پیشبالینی با مدلهای حیوانی برای ارزیابی ایمنی و اثربخشی
- ثبت درخواست به سازمانهای نظارتی (IND/CTA)
- کارآزماییهای بالینی در چهار فاز متوالی
- تحلیل نتایج، ثبت درمان، و نظارت پس از ورود به بازار
هر کدام از این مراحل، کیفیت و اعتبار علمی پژوهش را تضمین میکند و به ارتقای سطح دانش پزشکی و درمانی کمک میکند.


